器官晶片:在微型人體中,預見新藥的未來
你知道嗎?製藥公司與研究機構每年投入數十億的美金、數十年的時間來研發一款新藥物,但這些新藥就算通過了動物測驗,仍有高達九成在最終的人體臨床實驗中以失敗告終。這樣的失敗率不僅浪費大量的金錢,也讓許多病患反覆經歷希望與絕望。這樣的情況也反映了,過去研究所依賴的動物模型,並無法完全預測人類的生理反應,且在重視倫理、動物福祉的氛圍下,開發新技術來替代傳統的動物實驗顯得刻不容緩。所幸,最新的「器官晶片」技術將成為新的曙光,他不僅能重現各種細胞在人體內的功能性,更能系統細模擬人體內的微環境,將大幅提高試驗的準確性。
撰文|林泳亨
新藥開發的困境:動物模型的極限
在現代醫學中,儘管全球的製藥公司與研究機構每年投入數十億美元的經費和數十年的研發時間,但在每十種成功通過動物測試的候選藥物中,仍有高達九種,會在最終的人體臨床試驗中以失敗告終。在這些失敗中,約有六成源於藥物在人體上無法展現預期的療效,另有三成則是因為出現了無法控制的嚴重毒性。這樣的失敗率,不僅是金錢的巨大浪費,更意味著無數患者的等待落空。該結果說明了一個問題:數十年來研究所依賴的動物模型,終究無法完全預測人類的生理反應。羅非昔布 (Vioxx) 是一款曾被寄予厚望的止痛藥,它在多達九項針對小鼠和大鼠的動物研究中均顯示對心血管系統安全,甚至在其中六項研究中被發現具有心臟保護作用。然而,當它被廣泛應用於人類後,卻在全球造成了估計高達14萬例致命的心臟病發作和中風,最終在2004年被全面撤市。
除了準確度的缺陷外,動物實驗的負擔也極其沉重。根據歐洲的數據,一項重複給藥的毒理試驗成本約為49,390歐元,而開發單一的單株抗體藥物,平均需要投入九年時間與高達6.5至7.5億美元的經費。近年來,非人類靈長類動物的實驗成本更是飆升至每隻5萬美元,使研發負擔雪上加霜。與此同時,倫理的考量也日益高漲。國際間倡導的「3R」原則——替代 (Replacement)、減少 (Reduction) 與改進 (Refinement) 已逐漸從學術呼籲轉變為各國的強制法規。這股壓力正從學術界延伸至監管機構,美國食品藥物管理局 (FDA) 已在其2025年的路線圖中明確提出目標:希望在未來三到五年內,讓動物研究從臨床前測試的「常規」轉變為「例外」。這項宣示,為替代技術的發展提供了前所未有的強大政策推力。
技術的誕生:器官晶片如何重現人體微環境
正是在這個迫切需要變革的時間點,器官晶片 (Organ-on-Chip) 技術應運而生,提供了一個革命性的解決方案。這是一項結合微流體工程與細胞生物學的技術,其核心目標是,在一個體積很小的晶片上,重建一個微型、卻功能完備的人體器官。這些晶片通常由透明聚合物製成,內部利用微加工技術,蝕刻出比髮絲更細的微流體通道與細胞腔室。科學家會在這些腔室中培養人類來源的細胞,來源可能是病患的原生細胞,也可能是由誘導性多能幹細胞 (iPSC) 分化出的特定器官細胞。
器官晶片與傳統細胞培養的根本區別,在於它重現了人體內至關重要的「動態微環境」。傳統的2D培養是使細胞在一個平面靜態生長,難以體現在體內的動態環境。然而,器官晶片透過微流體通道,模擬了血液在微血管中的持續流動以及血液與細胞的交互作用。這股流動不僅帶來了養分、移除了廢物,更對細胞施加了精確的流體剪切力 (Fluid Shear Stress)。這種3D的類組織結構、動態的液體交換、以及多細胞的空間排列,使得細胞能夠在一個更接近體內的環境下存活數週甚至數月,並維持其高度分化的複雜功能,例如肝臟的代謝、腎臟的過濾或心臟的跳動。

器官的動力學:模擬呼吸與蠕動的關鍵突破
此技術真正的突破,在於它能精準模擬器官在體內的「物理性動力」。以肺臟晶片為例,美國Wyss研究所的科學家們設計了一種巧妙的結構,在中央細胞通道的兩側,各設置了一個可周期性抽真空的側通道。當真空啟動時,會使通道間的柔性薄膜產生規律的拉伸與舒張,完美模擬了人類呼吸時肺泡的機械性擴張。正是這種如呼吸般的物理拉伸,啟動了肺泡上皮細胞的先天免疫反應。暴露在這種機械應變下的肺晶片,使其S100A7蛋白表達顯著上調,從而能有效抑制禽流感乃至普通感冒冠狀病毒的感染。而這樣的防禦機制,是在靜止培養的細胞中觀察不到的,由此可見動態的環境對於重建體內的微環境的重要性。
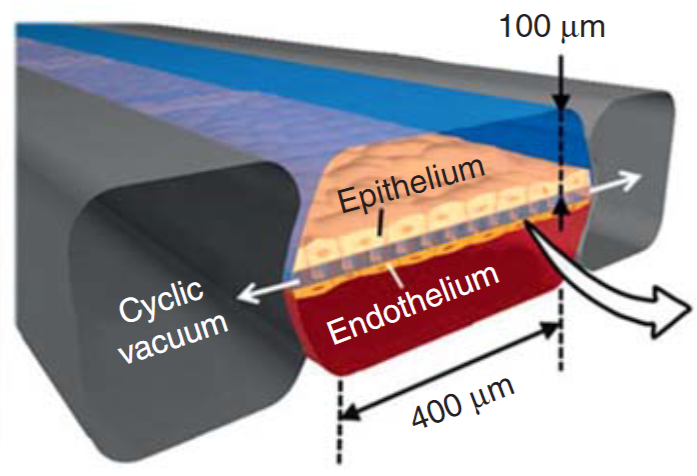
同樣的原理也應用於腸道晶片。透過對柔性多孔膜施加規律的周期性拉伸,科學家成功模擬了腸道規律的蠕動。在這種動態的機械刺激下,腸道上皮細胞會自發地停止增生,並分化、組織起來,生長成真實腸道中的絨毛狀結構。這種動態培養下的微型腸道,其屏障完整性和吸收功能,遠非傳統靜態培養所能比擬。這使得研究藥物吸收、營養代謝,乃至腸道菌群與宿主上皮的複雜互動,都變得更加貼近真實人體。
重建多細胞互動:異質性與功能性的提升
另外,實際上器官也並不是由單一細胞構成的,而是由多種細胞相互合作所形成的「細胞社會」。因此開發人員期待器官晶片具備重建這種多細胞狀態與交互作用的獨特能力。例如,一篇2024年發表於《Nature》的研究,展示了一個先進的心臟晶片。科學家在晶片上共同培養了三種細胞:心肌細胞、心臟纖維母細胞與血管內皮細胞。研究發現,這三種細胞共培養的微型心臟組織,其收縮力顯著高於僅有心肌細胞和纖維母細胞的組合,顯示內皮細胞對於心肌的功能性至關重要。這個微型心臟會自發性地規律跳動長達60天,並且對特定藥物產生與人體一致的生理反應;例如去甲腎上腺素會使其心跳加快,而鈣通道阻斷劑則會使其收縮力顯著下降。
肝臟是人體的解毒中心,絕大多數藥物都在此處代謝。傳統2D培養的肝細胞會迅速失去其代謝酵素活性,使其無法用於藥物毒性或代謝研究。然而,在微流體灌流的肝晶片上,這些細胞的代謝酵素活性得以長期維持。2022年發表於《Communications Medicine》的一項指標性驗證中,Emulate公司的肝臟晶片被用來測試一系列已知藥物,結果顯示,它能正確識別會對人類造成肝損傷的藥物。這些成果顯示,肝臟晶片已具備足以補足傳統模型不足的預測能力,並正逐漸成為評估藥物安全性的可靠工具。
感測與自動化:邁向智慧化的晶片平臺
器官晶片的能力還在不斷擴展。科學家們已開始整合微型生物感測器,打造具備即時監測能力的智慧晶片。一篇2017年發表於《PNAS》的研究,展示了一個完全整合的模組化平臺,晶片上不僅有控制流體的微控制器,還內建了監測pH、氧氣、溫度的物理感測器和可連續原位監測細胞分泌的生物標記的電化學感測器。該高通量平臺甚至能整合獨立的微型幫浦與經上皮電阻 (TEER) 感測器,讓研究人員能實時追蹤腸道或血腦屏障的完整性變化。

當這些獨立的器官晶片被串聯起來,一個更宏大的概念——「多器官晶片」。例如,一個「腸-肝晶片」系統可以精確模擬口服藥物的完整旅程:藥物首先在腸道晶片被吸收,其吸收的劑量與代謝物,隨後經由微流體通道送入肝臟晶片進行循前代謝 (presystemic metabolism)。研究者因此能精確評估藥物的口服生物利用度,以及代謝物可能對肝臟造成的次級毒性,在體外重現了複雜的全身性藥物動力學。
而近年來,製藥公司已開始積極採用晶片平臺進行早期藥物篩選,以便在投入成本進入動物試驗之前,就提早篩除無效或有毒候選藥物。而在2022年,美國國會通過了《FDA現代化法案2.0》,該法案正式授權FDA在審核新藥時,可以接受基於器官晶片等替代方法的數據,而不再強制要求動物試驗。隨後在2024年9月,Emulate公司的肝臟晶片S1,成為第一個被FDA正式接受並納入的器官晶片模型。這標誌著器官晶片已不再是實驗室中的概念,而是正式踏上了成為臨床前藥物評估標準工具的道路。
展望未來:個人化醫療與AI驅動的新方向
器官晶片技術正朝向更智慧化與個人化的方向前進。研究人員開始在晶片中加入各類微型感測器,用於即時監測細胞狀態,並結合人工智慧分析,讓藥物安全性與效果的預測更早、更精準。同時,利用患者來源的細胞建立「微型器官」,可在體外快速測試多種治療方案,提供與個別病患更相關的資訊,未來有機會成為臨床決策的輔助工具。隨著技術標準化與應用範圍擴大,器官晶片將逐漸成為新藥開發的重要平臺,並推動生物醫學從傳統動物模型轉向更有效率、更貼近人體生理的研究模式。器官晶片所代表的轉變,正讓我們從以動物模型為基礎的傳統途徑,走向更精準、更人道的生物醫學新時代。
參考文獻
- Van Norman, G.A., Limitations of animal studies for predicting toxicity in clinical trials: is it time to rethink our current approach? JACC: Basic to Translational Science, 2019. 4(7): p. 845-854.
- Marshall, L.J., et al., Poor translatability of biomedical research using animals—a narrative review. Alternatives to Laboratory Animals, 2023. 51(2): p. 102-135.
- Krumholz, H.M., et al., What have we learnt from Vioxx? Bmj, 2007. 334(7585): p. 120-123.
- Bottini, A.A. and T. Hartung, Food for thought… on the economics of animal testing. ALTEX-Alternatives to animal experimentation, 2009. 26(1): p. 3-16.
- Poh, W.T. and J. Stanslas, The new paradigm in animal testing–“3Rs alternatives”. Regulatory Toxicology and Pharmacology, 2024. 153: p. 105705.
- Ingber, D.E., Human organs-on-chips for disease modelling, drug development and personalized medicine. Nature Reviews Genetics, 2022. 23(8): p. 467-491.
- Zhao, Y., et al., Organs-on-a-chip: a union of tissue engineering and microfabrication. Trends in biotechnology, 2023. 41(3): p. 410-424.
- Bai, H., et al., Mechanical control of innate immune responses against viral infection revealed in a human lung alveolus chip. Nature communications, 2022. 13(1): p. 1928.
- Kim, H.J., et al., Human gut-on-a-chip inhabited by microbial flora that experiences intestinal peristalsis-like motions and flow. Lab on a Chip, 2012. 12(12): p. 2165-2174.
- Liu, Y., et al., Human heart-on-a-chip microphysiological system comprising endothelial cells, fibroblasts, and iPSC-derived cardiomyocytes. Scientific reports, 2024. 14(1): p. 18063.
- Ewart, L., et al., Performance assessment and economic analysis of a human Liver-Chip for predictive toxicology. Communications Medicine, 2022. 2(1): p. 154.
- Zhang, Y.S., et al., Multisensor-integrated organs-on-chips platform for automated and continual in situ monitoring of organoid behaviors. Proceedings of the National Academy of Sciences, 2017. 114(12): p. E2293-E2302.
- Wang, M., et al., Perfluoropolyether-based gut-liver-on-a-chip for the evaluation of first-pass metabolism and oral bioavailability of drugs. ACS Biomaterials Science & Engineering, 2024. 10(7): p. 4635-4644.
- Huang, Y., et al., From organ-on-a-chip to human-on-a-chip: A review of research progress and latest applications. ACS sensors, 2024. 9(7): p. 3466-3488.
- Polini, A., Prodanov, L., Bhise, N. S., Manoharan, V., Dokmeci, M. R., & Khademhosseini, A. (2014). Organs-on-a-chip: a new tool for drug discovery. Expert opinion on drug discovery, 9(4), 335-352.
