【創新技術】科學家找到完整機制對付核汙染地下水
■核能產生的地下水污染不僅汙染水源本身,其經過的土壤及周邊環境都會受到影響。那麼,我們能利用什麼機制將地下水中的鈾離子U(VI)去除呢?

撰文|方程毅
核能一直是個充滿爭議的能源,車諾比事件、福島核災甚至國內始終爭論不休的核四議題皆源自人類對輻射污染最深層的恐懼,縱使反核聲浪一波又一波,但在無法完全脫離核能倚賴的今天,總還是得想想辦法解決這個令人頭大的問題。
過往有學者指出當水中含有鈾離子時,六價鈾會與磷酸鹽類生成溶解度很低的化合物,例如:[  ]或[
]或[  ],因此能將鈾從水中固化,科學家嘗試將磷酸鹽直接加入鈾汙水中,但成效卻不彰,經深入研究後才發現鈣離子形成化合物[
],因此能將鈾從水中固化,科學家嘗試將磷酸鹽直接加入鈾汙水中,但成效卻不彰,經深入研究後才發現鈣離子形成化合物[  ]在水中的溶解度與理論有一段差距,因此科學家便開始懷疑鈣、磷酸根及鈾離子之間是否有其他反應機制尚未被發現,來自美國華盛頓大學 (Washington University in St. Louis)及西北太平洋國家實驗室 (Pacific Northwest National Laboratory) 的研究團隊便針對磷酸固鈾的機制做了一項完整的研究,發表在美國化學協會 Environmental Science & Technology 期刊上。
]在水中的溶解度與理論有一段差距,因此科學家便開始懷疑鈣、磷酸根及鈾離子之間是否有其他反應機制尚未被發現,來自美國華盛頓大學 (Washington University in St. Louis)及西北太平洋國家實驗室 (Pacific Northwest National Laboratory) 的研究團隊便針對磷酸固鈾的機制做了一項完整的研究,發表在美國化學協會 Environmental Science & Technology 期刊上。
一般來說鈾汙水pH值會在4-7.5之間,研究團隊利用實驗發現鈾離子與磷酸鈣的反應會根據pH值的變化,以及磷酸鈣一開始存在於水中的狀態而有所不同。磷酸鈣在pH為7.5的環境中溶解度相當低,但當pH值下降時溶解度便開始增加,但不管磷酸鈣是以固態還是離子態存在於溶液中,它都有辦法將鈾固化。
固化機制主要分為三個路徑:
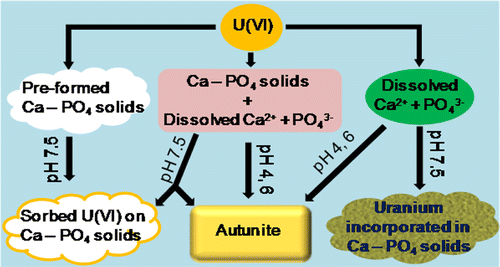
第一個路徑為「固態磷酸鈣吸附鈾」,磷酸鈣在pH為7.5的環境下會沉澱,而其固態狀可以將鈾離子「吸附」在固體上,接下來只要將固態磷酸鈣從水中撈出,鈾離子也就同時被帶離水中了
但當環境開始變為酸性,pH值降到6以下時,就開始走第二條路徑,這時會有部分磷酸鈣以離子形式(鈣離子及磷酸鹽離子)存在,鈾會與兩者反應,形成[  ]沉澱,[
]沉澱,[  ]是鈣鈾雲母(autunite)的主要成分,是存在於自然界的放射性礦物。溶液越酸就越傾向形成[
]是鈣鈾雲母(autunite)的主要成分,是存在於自然界的放射性礦物。溶液越酸就越傾向形成[  ]沉澱,若是接近中性則第一種機制的固態吸附也會同時存在。形成[
]沉澱,若是接近中性則第一種機制的固態吸附也會同時存在。形成[  ]沉澱同時也表示水中的鈾濃度下降。
]沉澱同時也表示水中的鈾濃度下降。
第三條路徑則是鈣離子和磷酸鹽離子在酸性環境以離子態存在於水中,但pH值開始上升時,磷酸鈣固體便會漸漸析出,析出的同時,鈾會取代部分原子鑲嵌其中,鈾離子也就隨著固體析出而脫離液體了。
這三個機制受到酸鹼度及個別離子濃度的影響,也因此不同環境下的固化機制大不相同,要解決地下水核汙染就必須針對不同狀態及所在地進行調整。但為什麼科學家對磷酸鈣系統特別有興趣呢?這是由於地下水本身即含有豐富的鈣離子,所以想要真正了解磷酸鹽類如何發揮作用就必須徹底了解磷酸鈣系統根鈾的反應機制。
指導這項研究計畫的Daniel Giammar教授表示:「這項研究成果顯示,並沒有任何單一方式可以解決地下水核汙染的問題。」「只要能掌握地下水遭受核汙染的區域以及地下水的成分,我們便可以決定要直接在受汙處注入磷酸鹽或是在其下游注入讓其形成磷酸鈣障蔽甚至是[  ]。」
]。」
原始論文:Mehta, V. S., Maillot, F., Wang, Z., Catalano, J. G., & Giammar, D. E. (2016). Effect of Reaction Pathway on the Extent and Mechanism of Uranium (VI) Immobilization with Calcium and Phosphate. Environmental science & technology.
參考資料及圖片出處:Trap and neutralize: A new way to clean contaminated groundwater
--
作者:方程毅 台大材料畢,目前於UCSD博士班掙扎中。科教中心特約寫手,從事科普文章寫作。
