嚴重特殊傳染性肺炎(COVID-19)治療藥物及預防疫苗的研發有何挑戰?
冠狀病毒 2019-nCoV(SARS-CoV-2)引發的嚴重特殊傳染性肺炎(COVID-19)已在全球大規模流行,確診及死亡人數不斷攀升,但迄無正式獲得核准上市的有效治療藥物及預防疫苗。為解決此人類本世紀最大公共衛生及健康危機,各國科學家莫不競相研發相關藥物及疫苗,有的已完成活體外實驗、進入動物實驗或正進行人體試驗中,期望在最短時間內完成測試提供臨床使用。目前,雖已有多種候選藥物可供患者使用,亦有很多疫苗正在進行試驗中,但仍有諸多挑戰有待克服。
撰文/陳淵銓
●潛在有效治療藥物:
1. 藥品:彙整國內外嚴重特殊傳染性肺炎(Coronavirus disease 2019, COVID-19)的相關研究報告,發現許多化學品、細胞激素(cytokine)及抗體(antibody)可能是治療COVID-19的潛在候選藥品(表1)。
表1. 潛在候選藥品清單
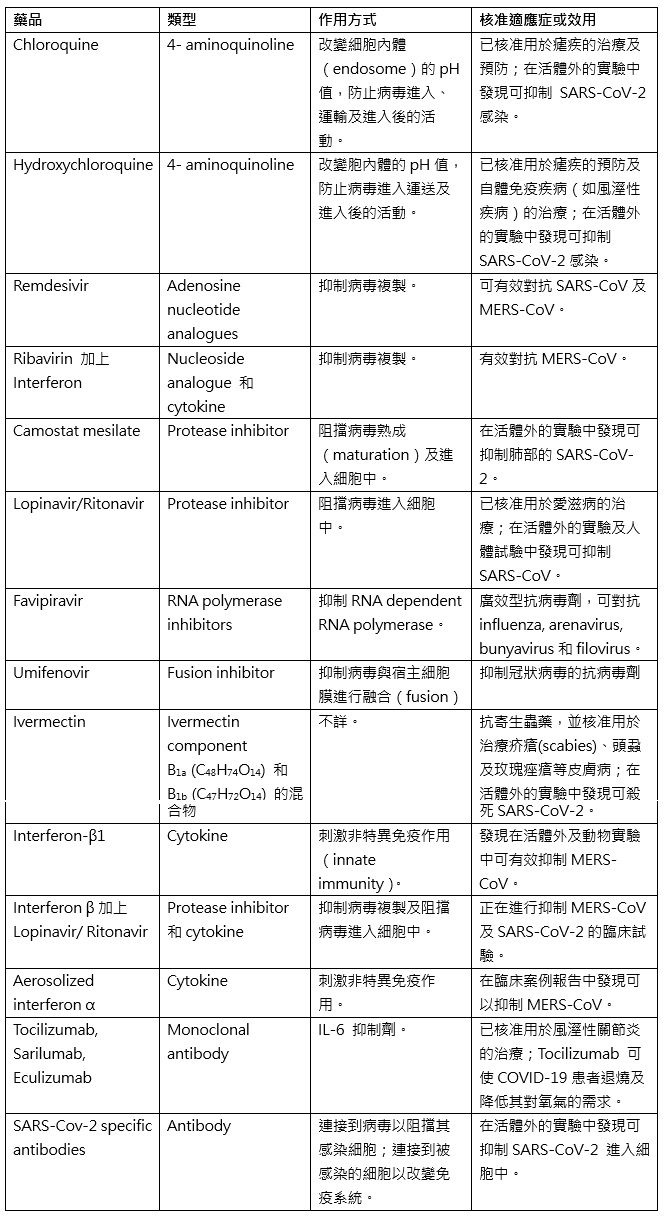
研發上的主要挑戰:
.大多僅進行活體外及動物實驗,尚未完成臨床試驗三期,臨床應用效果及可能的不良反應(副作用)並未充分評估。
.COVID-19患者的症狀可大致分成無症狀、輕症及重症三種,並未評估個別藥品對不同程度症狀患者的適用性,例如:Chloroquine及Hydroxychloroquine適用於輕症,Remdesivir 適用於重症。
.SARS-CoV-2 的RNA基因組突變率高,已發現有多種變異株產生,恐怕會有抗藥性病毒株出現的可能。
2. 特殊生物製劑(痊癒者的血漿)
在2020年,中國醫師抽取5位COVID-19痊癒者的血漿(convalescent plasma),血漿中的SARS-CoV-2特異性抗體(IgG)結合效價(binding titer)大於1:1000,中和效價(neutralization titer)大於40,輸血給呈現嚴重急性呼吸綜合症候群(severe acute respiratory syndrome, ARDS)的COVID-19重症病人,在10至22天給予痊癒者的血漿,發現在5例患者中有4例在3天內體溫恢復正常,病毒負載量也下降;輸血後第12天,有4例患者的ARDS消失;在治療14天內,有3例患者不再需要使用呼吸器。在5名患者中,有3名可分別在住院53、51和55天後出院,還有2名在輸血後第37天病情穩定,顯示給予包含中和抗體的痊癒者的血漿可改善病人的臨床症狀。
研發上的主要挑戰:
.案例數僅有5例呈現ARDS的COVID-19重症患者,本研究應僅為案例報告(case report),並未完成全部臨床試驗,此種療法可能僅適用於瀕危的重症患者。
.未評估接受痊癒者血漿的COVID-19患者是否有排斥及過敏的現象,預後(prognosis)情況亦無持續追蹤評估之報告,。
.未考量痊癒者是否患有其他疾病,其血漿中除有抗體外,可能還含有其他物質甚至微生物,未進行治療利益及風險評估。
●預防疫苗的研發
在2020年,香港研究人員基於SARS-CoV-2與SARS-CoV具有高度遺傳相似性,利用現有的SARS-CoV免疫學研究資料,以設計對抗SARS-CoV-2的疫苗。他們鑑定了一組得自病毒棘突蛋白(spike protein)和核殼蛋白(nucleocapsid protein)的B細胞和T細胞抗原表位(epitope),在120個可用的SARS-CoV-2序列中,並未觀察到在已確定的抗原表位發生突變,所以疫苗若免疫標靶作用於這些抗原表位,應可提供人體保護以對抗SARS-CoV-2。
研發上的主要挑戰:
.疫苗乃提供與健康人作疾病預防之用,安全性要求標準極高,僅有活體外實驗成功,證據仍顯不足,須經長期及大量的動物實驗及健康自願者試驗方能完成安全性及有效性測試。
.病毒突變率高,棘突蛋白和核殼蛋白的保守性(conservation)未作詳細評估,疫苗有效性(effectiveness)及效期(expiration)可能均相當有限。
.根據現有臨床資料顯示,病毒株已發生突變而可能是兩種以上的混合株(mixed population),針對單一病毒株抗原研發的疫苗恐無法提供人體完整免疫力。
參考資料:
- Singh AK, Singh A, Shaikh A, Singh R, Misra A. Chloroquine and hydroxychloroquine in the treatment of COVID-19 with or without diabetes: A systematic search and a narrative review with a special reference to India and other developing countries. Diabetes Metab Syndr. 2020 Mar 26;14(3):241-246. doi: 10.1016/j.dsx.2020.03.011. [Epub ahead of print]
- Shen C, Wang Z, Zhao F, Yang Y, Li J, Yuan J, Wang F, Li D, Yang M, Xing L, Wei J, Xiao H, Yang Y, Qu J, Qing L, Chen L, Xu Z, Peng L, Li Y, Zheng H, Chen F, Huang K, Jiang Y, Liu D, Zhang Z, Liu Y, Liu L. Treatment of 5 critically Ill patients with COVID-19 with convalescent plasma. JAMA. 2020 Mar 27. doi: 10.1001/jama.2020.4783. [Epub ahead of print]
- Wang M, Cao R, Zhang L, Yang X, Liu J, Xu M, Shi Z, Hu Z, Zhong W, Xiao G. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Res. 2020 Mar; 30(3):269-271. doi: 10.1038/s41422-020-0282-0. Epub 2020 Feb 4.
- Du YX, Chen XP. Favipiravir: pharmacokinetics and concerns about clinical trials for 2019-nCoV infection. Clin Pharmacol Ther.2020 Apr 4. doi: 10.1002/cpt.1844. [Epub ahead of print]
- Ahmed SF, Quadeer AA, McKay MR. Preliminary identification of potential vaccine targets for the COVID-19 coronavirus (SARS-CoV-2) based on SARS-CoV immunological studies. Viruses. 2020 Feb 25;12(3). pii: E254. doi: 10.3390/v12030254.
