【細胞世界】發現回撥老化時鐘的新方法

撰文|葉綠舒
返老還童,或是長生不老,是許多人的夢想。即使是秦始皇,也希望能夠長生不老。而坊間那麼多的「抗老化」秘方,不也說明了現代人希望青春永駐?沒有人喜歡「視茫茫,髮蒼蒼,齒牙動搖」,即使那是不得不然,也希望能夠盡可能地延緩。
因此,近代科學也一直致力於找到老化的關鍵。最近,史丹佛大學醫學中心(Stanford University Medical Center)發現,將端粒酶(telomerase)的mRNA(信息RNA)經過修飾後注入細胞,可以延緩老化。
端粒酶是帶有核糖核酸(RNA)的酵素。它的功能是在染色體末端加上「TTAGGG」的重複序列(稱為端粒telomere)。端粒酶自己的RNA,與染色體末端的TTAGGG序列互補,在染色體末端加入更多的TTAGGG重複(如下圖)。
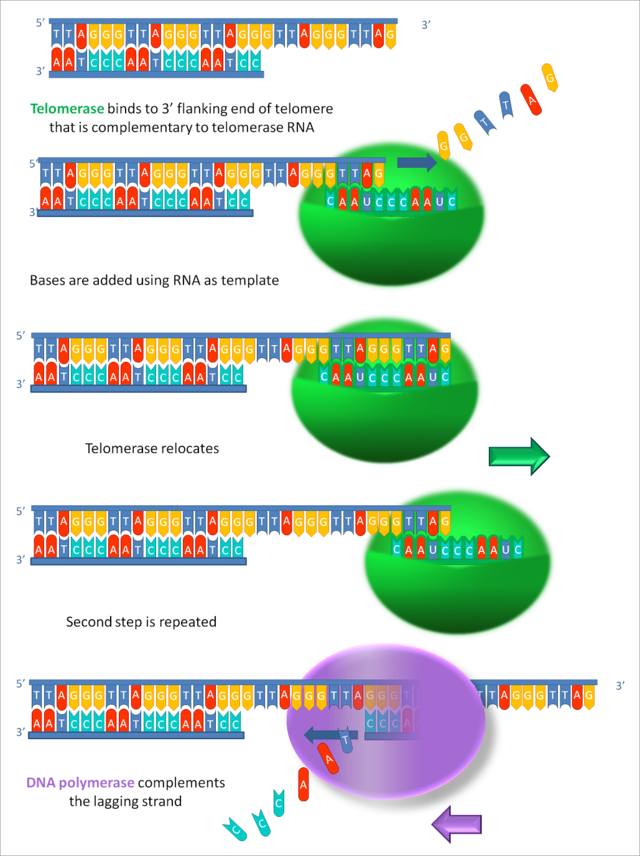
為什麼需要端粒酶在染色體末端加入重複的序列呢?說來話長,原來,合成染色體的酵素--DNA 聚合酶(DNA polymerase),在合成新的DNA時,需要有範本(template)與引子(primer),並且一定要由5'磷酸根往3'氫氧根的方向,來合成新的一股的DNA(如下圖)。
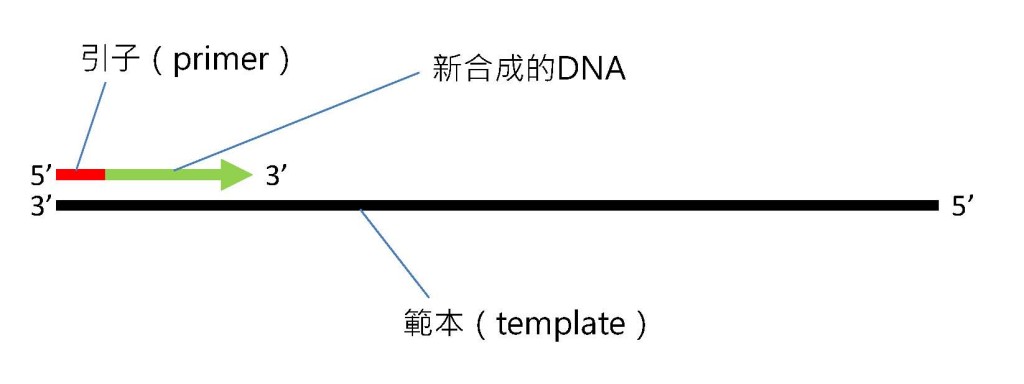
但是,染色體原來就是由兩條DNA(去氧核糖核酸)5'端(5'磷酸根)對3'端(3'氫氧根)構成的(由上圖也可以看到),這樣的構造稱為雙股反平行。雙股反平行的構造,使得染色體非常穩定,不容易受到環境中的酸與鹼破壞而失去活性。但是,當DNA聚合酶在合成新的染色體時,由於染色體雙股反平行的構造,使得打開的兩股,其中一股的方向與DNA聚合酶合成的方向相反。
如上圖,圖片下方的那一股DNA,因為方向就是從3'端到5'端,所以DNA聚合酶可以從DNA的最前端開始複製到最末端。但是圖片上方的那一股DNA(稱為延遲股,lagging strand)要怎麼辦呢?
由於DNA聚合酶不可能反向複製,當時有人提出:延遲股DNA的複製方式,是斷斷續續的複製(如下圖)。而這個假說,由岡崎令治(Reiji Okazaki)在1968年證實了。
的複製方式-1024x699.jpg)
岡崎令治以巧妙的實驗,分離出片段的DNA,證實了這個假說;為了紀念他,這片段的DNA便稱為岡崎片段(Okazaki fragment)。
不過,解決了這個問題,接著來的是下一個問題。當DNA複製終了時,如果是環狀的DNA(如細菌等原核生物),最後留下的缺口可以很容易地補上;但線狀DNA(如我等真核生物)的複製,到了DNA的最末端時,會因為無法產生引子(對,引子也是由特殊的酶合成的),造成合成的DNA「長短腳」(如下圖)。

這個假說,在1973年由歐洛尼可夫(Alexey Olovnikov)提出。當時,他也提出生物一定有相對應的機制來彌補這個長短腳的問題。而Carol W. Greider, Elizabeth Blackburn 與 Jack W. Szostak在 1984年證實了端粒酶的存在。
端粒酶在染色體末端加上「TTAGGG」重複的序列,於是在複製時的「長短腳」問題便不那麼令人擔心了。畢竟,失去的只是重複的序列,而且,還有端粒酶來補充。
但是,即便有端粒酶,科學家們發現,隨著細胞一次次的分裂,染色體一次次地複製,端粒還是愈來愈短。最後,細胞便不再能分裂,走入老化、死亡。
科學家們一直在試圖找出可以延緩端粒變短的方法。過去曾有人嘗試將負責產生端粒酶蛋白質部分(telomerase reverse transcriptase,簡稱TERT)的mRNA放入細胞,使端粒酶的表現量升高,來造成端粒延長;結果卻產生了針對端粒酶的免疫反應。這次,史丹佛的研究團隊使用了修飾過的TERT的mRNA,使細胞中的端粒酶的量只提高了24到48小時,避免了免疫反應的發生,使得細胞的端粒被延長了900個鹼基對(base pairs,為計算DNA大小的單位)。
端粒延長900個鹼基對有什麼效果呢?研究團隊發現,當纖維母細胞(fibroblast,可發育為皮膚細胞)的端粒被延長後,它可以多分裂28次,這樣可以產生上千億個細胞;而肌母細胞(myoblast,可發育為肌肉細胞)可以多分裂3至4次。由於這個方法只是讓端粒酶的活性短暫地提高,過後細胞又繼續正常的老化,是不是很類似於將時鐘回撥一樣呢?
參考文獻:
2015/1/23. Telomere extension turns back aging clock in cultured human cells, study finds. Science Daily.
John Ramunas, Eduard Yakubov, Jennifer J. Brady, Stéphane Y. Corbel, Colin Holbrook, Moritz Brandt, Jonathan Stein, Juan G. Santiago, John P. Cooke, and Helen M. Blau. 2015. Transient delivery of modified mRNA encoding TERT rapidly extends telomeres in human cells. FASEB J. doi: 10.1096/fj.14-259531
--
作者:葉綠舒 慈濟大學生命科學系助理教授,科教中心特約寫手,從事科普文章寫作。
