【關於 COVID-19 的這大半年】檢驗上的兩三事
轉眼間,2020 年夏天就這樣來了。大半年裡,「嚴重特殊傳染性肺炎」COVID-19 (亦稱武漢肺炎)的疫情席捲全球,如今依然張狂。而台灣,像個世外桃源。接下來,在這一系列專題裡,我們就一起來討論這大半年裡,在臨床與研究前線上,我們對於這惡名昭彰的 COVID-19 與罪魁禍首 SARS-CoV-2,各界專家窮盡心力所慢慢搞清楚(或是還沒弄明白)地這些那些事吧。讓我們一起來以疫情為基,好好地討論免疫學吧!
撰文/駱宛琳
首先,在開始討論病毒特性、免疫反應、疫苗進展、與藥物開發之前,我們先來聊聊關於 SARS-CoV-2 病毒檢測上的一些事情。
目前,最常被討論用來檢測 SARS-CoV-2 病毒的兩種檢測方法,分別是以分子生物學核酸為本的 RT-qPCR 試驗,以及血清學檢測(serological test)。兩種測驗能透露的訊息不太一樣。RT-qPCR 為主的檢測,旨在把 SARS-CoV-2 這現行犯,在犯罪現場抓個正著。而血清學檢測,則很像是去警調單位去探查 SARS-CoV-2 的過往犯罪史。
RT-qPCR 檢測常常被簡稱為PCR,雖然以科學嚴謹度來說,這種簡稱不太正確,但意義算是有到。所以如果在日常裡聽到,算是同種檢測,可以將就一下。為什麼說 RT-qPCR 檢測可以將現行犯 SARS-CoV-2 在犯罪現場逮個正著呢?
SARS-CoV-2 說到底,畢竟是個病毒。SARS-CoV-2 本身隸屬於冠狀病毒科(Coronavirinae)。病毒名裡頭的 「CoV」,就是冠狀病毒的意思。SARS-CoV-2 雖然這次殺得人類措手不及,歷史上,我們和冠狀病毒的交手卻絕非史無前例。有些會造成尋常感冒症狀的病毒,就同樣也是隸屬於冠狀病毒科,但在感染人類之後,殺傷力比較輕微,算是科裡的無名小卒。但,人外有人,冠狀病毒科裡面,也有殺手級的角色。像是 2003 年在台灣爆發疫情的 SARS 重急性呼吸道症候群冠狀病毒,還有2015 年在韓國肆虐的 MERS-CoV 中東呼吸症候群冠狀病毒,就是令人髮指的角色。
既然 SARS-CoV-2 畢竟是個病毒,其身家起底,也自然也就有著病毒的特徵。一如冠狀病毒科的其他病毒,SARS-CoV-2 外頭包著外套膜,圓鼓鼓的,帶著許多突起。那些突起因為狀似皇冠,而讓這科病毒因此得此名。這些皇冠狀突起對冠狀病毒來說,是感染細胞的武器,接下來也會好好介紹。除此之外,冠狀病毒還是單股、正鏈、RNA病毒。而 RT-qPCR 檢測,就是將矛頭對準SARS-CoV-2 所獨有的 RNA 序列。SARS-CoV-2 所帶有的獨特 RNA 序列,就像其獨屬的病毒指紋。但是,比在犯罪現場搜找罪犯指紋要慶幸的是,RT-qPCR 的檢測要靈敏太多了。
但這靈敏性,卻也是 RT-qPCR 檢測的阿基里斯腱。
我們先來妄想一下,如果可以跟阿拉丁神燈許願一種能夠讓 SARS-CoV-2 無所遁形的檢測,來拯救好可憐的 2020 年,你會如何跟神燈說呢?
我覺得,來跟神燈求一種,能夠既「靈敏」又「準確」地篩檢出具有把 SARS-CoV-2 「傳染給其他人危險性」的感染者,如何?
為什麼這三項特點很重要呢?首先,當前疫情危難裡,篩檢測驗的最主要目標,是能夠篩出具有傳染性的感染者。檢測要既靈敏又準確,這比較好理解。我們希望檢測讓病毒無所遁形(靈敏度高),同時,檢測結果還要能夠被絕對信賴(專一度高)。
不過,越來越多的臨床數據顯示,不是所有人在感染 SARS-CoV-2 之後都會出現讓患者「意識到」自己出現類似於感冒的症狀。可嘆的是,呼吸道症狀的嚴重程度,似乎和感染者的傳染力度,沒有直接關聯。而是和感染的時間軸比較有關。
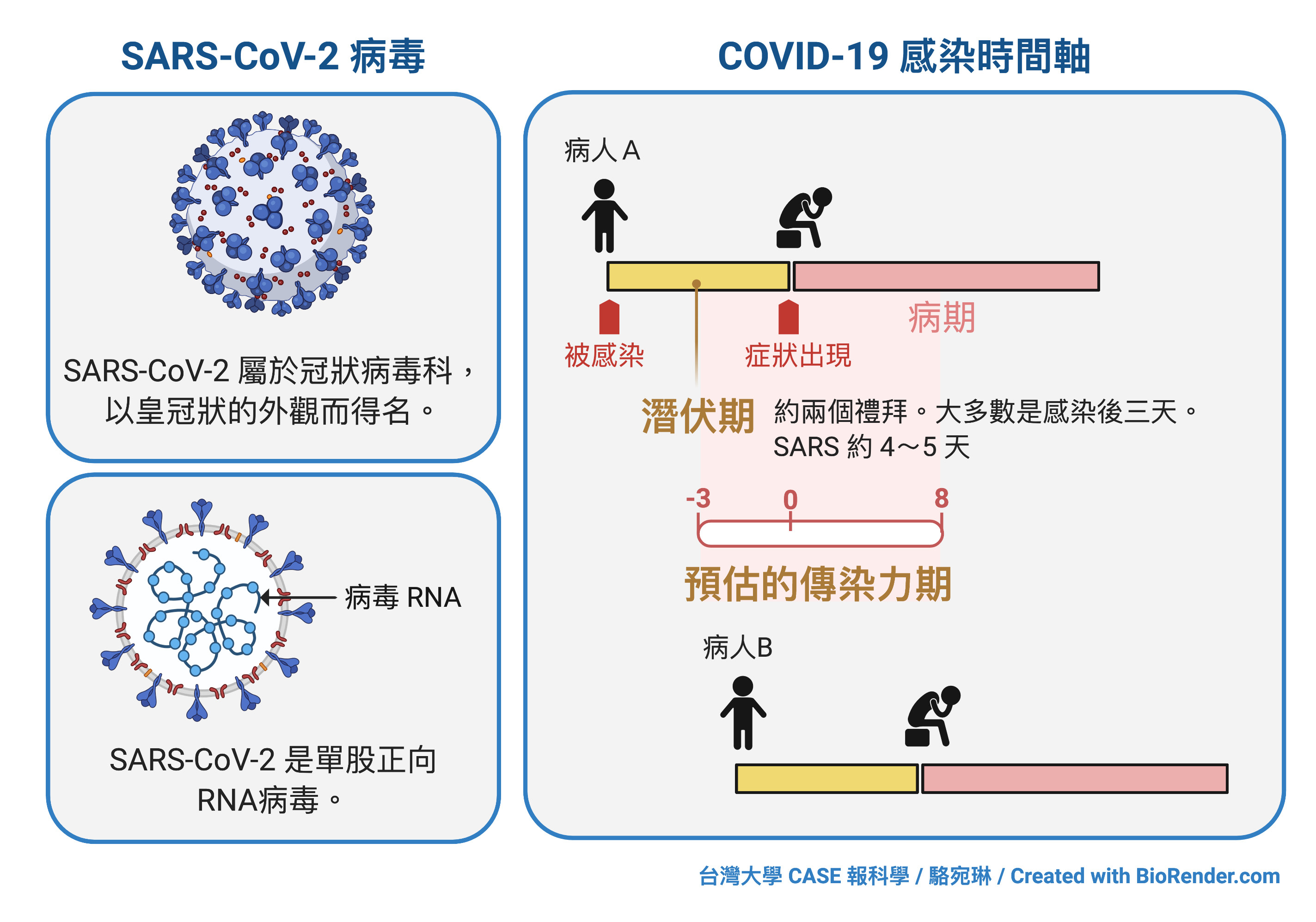
這是什麼意思呢?目前,科學家與醫療界的共識是,傳染力(transmissibility)和病毒量(virus load)有著絕對正比關係。帶原的病毒量愈多,該個體的傳染力就會愈驚人。而病毒量多寡,則和被感染的時間軸有明顯相關。
病毒量對感染傳播力的重要性,也直接影響到防疫宣導相關的政策宣導。這也的確是為什麼要耳提面命地一再提醒大家,絕對要勤洗手、不摸臉、乖乖戴口罩、努力保持社交距離。因為,接觸的病毒量愈少,被感染的機會就愈少;接觸的病毒量愈少,感染症狀也會比較輕微喔。你說這是不是一石好幾鳥,保護自己也保護眾人呢。
但,這也讓檢測結果這非黑即白的是非題,無法提供一個完美地、能夠一翻兩瞪眼的絕對正確答案。
在個體被感染之後,目前覺得症狀出現前就有感染力,但最讓人揪心皺眉頭的,還是在症狀出現的五到八天內。各地方的數據雖然多少有點差異,但大抵脫不出這範圍。我們可以來瞧瞧台灣自己出品的一篇漂亮研究。由武漢肺炎疫情研究小組(Taiwan COVID-19 outbreak investigation team)與台灣大學公共衛生學院林先和教授實驗室、與疾病管制署攜手合作,在 Jama Internal Medicine 上發表了一篇以台灣疫情數據為基礎,對傳染力的分析研究。
這篇研究裡,統計追蹤了一月中到三月中,接觸到確診個案而需居家隔離十四天的人。在一百位參與研究的確診病人裡,共追蹤了兩千七百多位和確診病患有密切接觸者。其中, 因為密切接觸而被感染的比例約為 0.7 %,但如果仔細分析這些人與確診病患的接觸史,會發現確診病患的感染時間軸,對傳播力有著非常關鍵的角色。最危險的時候,大概是確診患者出現臨床症狀的五天以內,還有症狀出現之前;在較晚的時間點接觸到確診病患,傳染力就相對小很多很多。
回到 RT-qPCR 檢測。目前的檢測的確讓人自豪;不僅篩驗時程所需時間愈來愈短,而且超級靈敏。但為什麼這超級強悍的靈敏度,會是個問題呢?
因為,在臨床症狀出現之後的五個禮拜內,都被發現很有可能會出現檢驗陽性的結果啊。很多時候,患者的臨床症狀也都早已消彌痊癒。而且大部分對病患的追蹤篩檢,發現從症狀出現,到檢驗結果陰性的所需時間,中位數大致介於 24 天左右。對於年紀比較大、或是有糖尿病、高血壓病史的病患,也被發現需要更多的時間,才能夠得到陰性檢驗結果。甚至,屢屢也有報導,發現就算連續兩次檢驗結果陰性,之後還是很有可能出現陽性。
這麻煩處正在於,檢驗結果嘗試用「是」、與「不是」來提供檢疫上的判斷基準,但往往沒有提供病患病毒量的資訊。
有趣的是,其實病毒量的資訊,正悄悄埋藏在 RT-qPCR 檢測裡。
RT-qPCR 檢測怎麼做呢?讓我們來假設,檢驗中心收到了一個被感染患者的檢體。首先,SARS-CoV-2 病毒的 RNA 會先被反轉錄、生成 DNA (RT 步驟),然後,在 qPCR 這一步實驗流程裡,被偵測的核酸序列訊號會被一步又一步,隨著 PCR 的實驗流程而被逐漸放大,過程裡的螢光訊號,可被我們讀取。神奇地是,螢光訊號會和「需要」被偵測的核酸量成正比,這也是為什麼能夠提供「定量」的訊息(也就是那個『q』)。換句話說,如果檢體裡一剛開始的病毒 RNA 量多,在一步又一步的放大流程裡,螢光訊號就會被急劇放大。跟病毒量少的檢體比較起來,病毒量「多」的檢體需要比較「少」的放大步驟數,就可以將我們想要偵測的核酸序列訊號(也就是讀取的螢光訊號)放大到一定程度。這個放大步驟數以比較科學的專業術語來描述,就是 Ct 值。而Ct 值所指得,是跨過閾值所需要的循環步驟數目(threshold cycle value)。Ct 值每增加 3.3,最初檢體裡的病毒量,就少十倍。而 Ct 值愈低,病毒量就愈多。
你發現其中的關鍵了嗎?重點不單是陰性還是陽性,還有,需要多少循環步驟,能夠有效地將病毒核酸序列放大到一定程度。通常在一定 Ct 值內,會被判定陽性反應。台灣目前所採取的界線是 Ct 值需低於 35。
在目前追蹤確診病患的文獻報告,常常發現在後段的幾個禮拜時間裡,Ct 值都偏高,甚至介於該國判斷陰性還是陽性的邊界上,而這也往往代表檢體裡的病毒量已經很低。
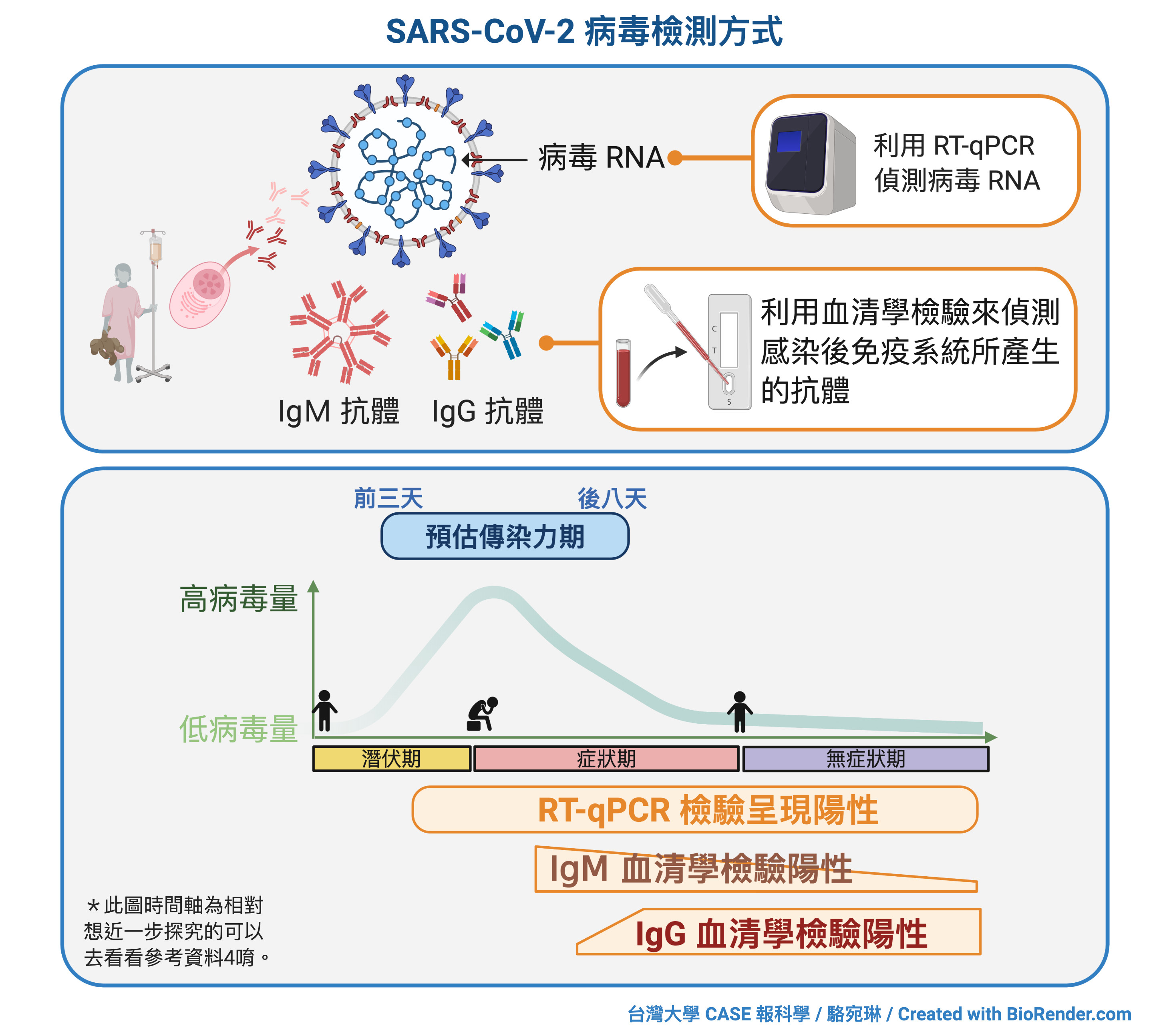
換言之,RT-qPCR 檢測非常重要,尤其在早期個案追蹤裡,能夠協助防疫上的判斷。但也需要記住的是,RT-qPCR 檢測結果,和個體是不是仍然具有感染力,卻不一定能夠直接劃上等號。這是因為 RT-qPCR 檢測實在是太敏感了,是抓 SARS-CoV-2 現行犯的絕佳偵探。但這偵探,有個狗鼻子,雖然能夠嗅出 SARS-CoV-2,但因為實在是太敏感了,如果這現行犯已經死了、或是喪失行動能力了,還是難逃那動一動就能夠嗅出不對勁的狗鼻子。
而相較於 RT-qPCR,血清學檢測則是把矛頭指向個體的病毒感染史。血清學檢測的假設很簡單,所謂凡走過必留下痕跡。而病毒感染,也是一樣。只要免疫系統沒有疲弱而對病毒視而不見,免疫系統不會坐之不理。免疫系統一旦啟動,先天免疫與後天免疫系統都會加入對抗病毒的作戰,並且遵照一定的啟動流程。而血清學就是根據我們對免疫系統啟動流程的理解,來監看對 SARS-CoV-2 的免疫力,來判斷個體是不是曾經被感染。後天免疫系統所需反應時間較長,大約要五到七天才能夠被啟動,但能夠提供免疫力。在這段時間裡,個體能夠產生抗體 IgG 所需的時間,又比 IgM 要長。因此,篩檢是不是具有對 SARS-CoV-2 有專一性的 IgG 抗體,可以大概推測出個體是不是曾經感染過。
總而言之,qRT-PCR 檢驗也好,血清學檢驗也好,是各有千秋與擅場,能夠提供的感染病資訊也有差異。端賴的是,是不是能夠對檢驗結果,好好地解讀喔。
參考資料
- Hao-Yuan Cheng, Shu-Wan Jian, Ding-Ping Liu, Ta-Chou Ng, Wan-Ting Huang, Hsien-Ho Lin, Taiwan COVID-19 Outbreak Investigation Team. Contact Tracing Assessment of COVID-19 Transmission Dynamics in Taiwan and Risk at Different Exposure Periods Before and After Symptom Onset. JAMA Intern Med. 2020 May 1;e202020. doi: 10.1001/jamainternmed.2020.2020. Online ahead of print.
- Xi He, et al. Temporal dynamics in viral shedding and transmissibility of COVID-19. Nat Med. 2020 May;26(5):672-675. doi: 10.1038/s41591-020-0869-5. Epub 2020 Apr 15.
- Michael R Tom and Michael J Mina. To Interpret the SARS-CoV-2 Test, Consider the Cycle Threshold Value. Clin Infect Dis. 2020 May 21 : ciaa619.
- Antonio La Marca, et al. Testing for SARS-CoV-2 (COVID-19): a systematic review and clinical guide to molecular and serological in-vitro diagnostic assays. Reprod Biomed Online. 2020 Jun 14;S1472-6483(20)30318-7. doi: 10.1016/j.rbmo.2020.06.001. Online ahead of print.
