偕二醇
偕二醇
國立臺灣師範大學化學系學士班一年級范智傑
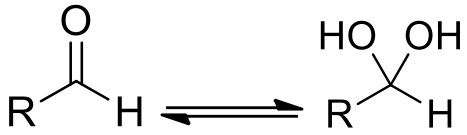
偕二醇是同一個碳上接有兩個羥基 (hydroxyl) 的有機化合物。一般來說是羰基水合的產物,它和羰基之間存在平衡關係(如圖一)。
影響偕二醇比例的原因:
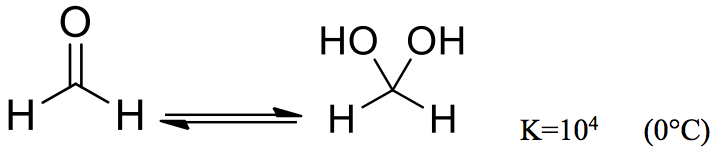
羰基旁的取代基 (substituent) 會影響到羰基上碳的電子密度。在沒有取代基的情況下,也就是甲醛 (methanal),偕二醇的比例是非常高的,事實上在甲醛的水溶液中是幾乎沒有甲醛單體的,拉曼光譜 (raman spectroscopy) 也無法觀察到羰基的蹤跡。
1950 年代,Iliceto、Trumpler、Bieber 等人利用其他分析方法得到甲醛水合的平衡常數 \(0^\circ C\) 時 \(=10000\),\(30^\circ C\) 時 \(=57000\),\(64^\circ C\) 時 \(=301000\)。
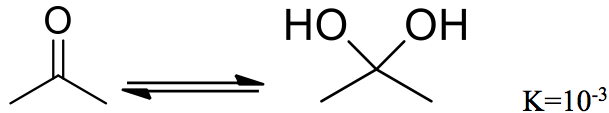
乙醛的部分因為有烷基推電子的關係,羰基的碳上電子密度 (electron density) 上升,等於幫助羰基穩定自己的正電荷,比較不需要吸引氧的孤對電子 (lone-pair electrons) 形成偕二醇以取得更多電子密度,乙醛水溶液中偕二醇的比例已經小於百分之一。丙酮 (acetone) 有兩個烷基推電子,羰基上的碳電子密度更高,偕二醇的比例就更低了(如圖二)。
相反的,當取代基為三氯甲基 (trichloromethyl-),也就是三氯乙醛 (trichloroethanal) 時,因為三氯甲基具有拉電子的效果,使羰基電子密度下降,比沒有取代基的甲醛更容易水合。甲醛形成的甲二醇 (methanediol)是無法分離的,也就是說甲醛一旦蒸發就是以單體的形式存在。
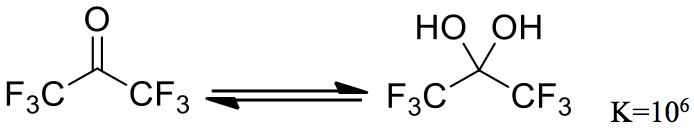
三氯乙醛的水合物比甲醛水合物更穩定,是可以分離的。其他的吸電子取代基如三氟甲基 (trifluoromethyl-) 等也有類似的效果,由兩個三氟甲基當取代基的六氟丙酮 (hexafluoroacetone),水合的平衡常數已經達到一百萬,無水物在空氣中會快速潮解(如圖四)。
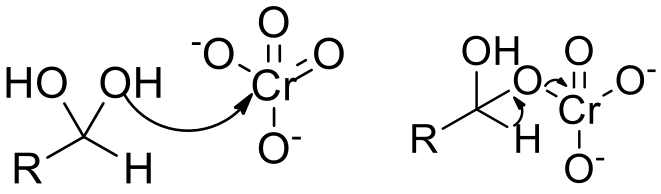
偕二醇和醛氧化的關係:醛類羰基上的碳本身是缺電子的,利用氧的孤對電子氧化也不容易。醇被氧化的過程中如果到醛的時候無法被溶劑化形成二醇或其他有羥基的結構,便不再繼續氧化成酸,停留在醛(如圖五)。
同樣使用六價鉻當氧化劑,在二甲基甲醯胺 (N,N-dimethylmethanamide) 和二氯甲烷 (dichloromethane) 中反應的結果不同,因為二甲基甲醯胺能像水一樣與醛化合,形成類似二醇的結構,進一步氧化成酸;二氯甲烷沒有這樣的能力,醇氧化到醛的時候就停止了,不再繼續氧化。
醛在水溶液中的還原力和偕二醇的比例是有關連性的,在與斐林試劑 (fehling’s solution) 反應的過程中,反應速率是甲醛>乙醛。大部分的情況下醛與斐林試劑反應時,斐林試劑中的二價銅離子會被還原成一價的氧化亞銅,甲醛的還原力比其他的醛強,有能力將二價銅離子還原成零價的金屬銅。
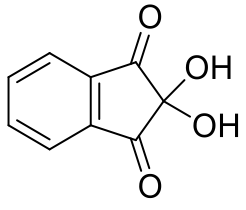
茚三酮 (2,2-dihydroxyindane-1,3-dione),一種常用於檢驗氨、一級胺、二級胺、胺基酸的化合物,以水合的形式存在。大部分的醛酮都是形成水合物後較不穩定,茚三酮發生反應的那個羰基因為周圍有兩個羰基吸電子,降低其電子密度,較容易水合形成偕二醇,穩定度反而比酮的形式還高(如圖六)。
羰基碳上缺電子是這個基團發生反應的重要原因,越缺電子就越容易和親核基 (nucleophile) 反應,水只是眾多親核基的其中一種,也是反映這個化合物中羰基活性的指標之一。
參考資料
- 胡躍飛主編,現代有機合成試劑(1)氧化反應試劑,化學工業出版社P10~11
- J.Frederic Walker,Formaidehyde,Third Edition,P79~84
- http://en.wikipedia.org/wiki/Geminal_diol
- http://chemwiki.ucdavis.edu/?title=Organic_Chemistry/Aldehydes_and_Ketones/Reactions_of_Aldehydes_%26_Ketones/Addition_of_Water_to_form_Hydrates_(Gem-Diols)
- http://en.wikipedia.org/wiki/Ninhydrin


 前一篇文章
前一篇文章 下一篇文章
下一篇文章
