丙二酸酯合成法(Malonic Ester Synthesis)
丙二酸酯合成法(Malonic Ester Synthesis)
國立臺灣師範大學化學系三年級俞姿宇
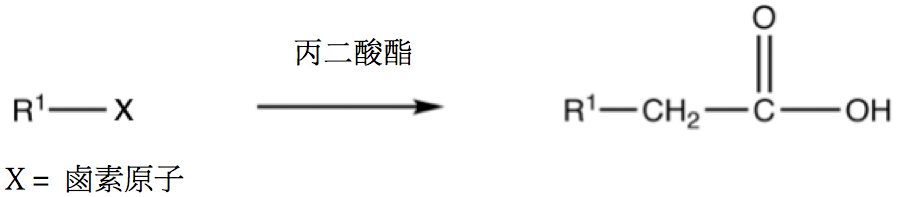
丙二酸酯合成法是一種有機合成法,將鹵烷類化合物轉變為羧酸化合物並增加兩個碳原子。是利用丙二酸酯(1)$$\alpha$$ 位置上有酸性較大的氫(2)易發生脫羧反應等兩大特性。
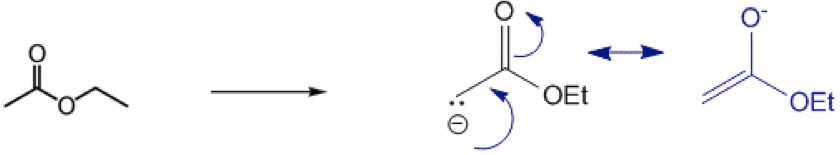
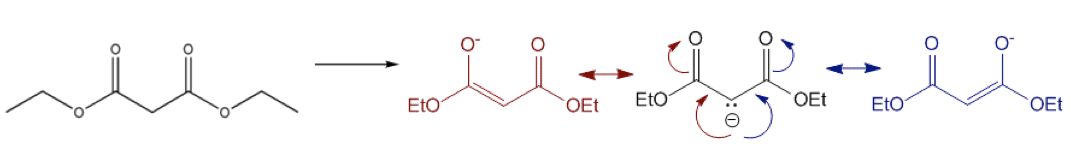
一般的酯類(圖一),脫去一個氫後,負電荷能共振到羰基的氧上;而脫去一個氫的丙二酸酯(圖二),負電荷則可被分散到一個碳原子及兩個氧原子上,共有三個共振式。電荷越分散、非定域化(delocalized)的程度越高,對其結構穩定度越有幫助。
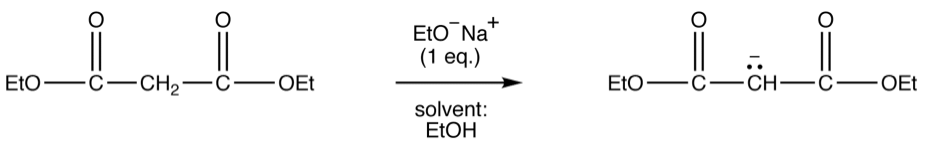
由於丙二酸酯脫掉氫後會得到雙邊共振穩定的烯醇鹽(enolate),丙二酸酯比一般的酯類酸性高了許多,所以可選用鹼性較弱的 NaOEt $$(pKa=16)$$,即能脫除丙二酸酯上的氫。在此所選用的鹼和溶劑通常和酯類上的烷氧基相同,避免發生酯交換反應,生成新的酯,增加產物的複雜性而難以分離。(圖三)
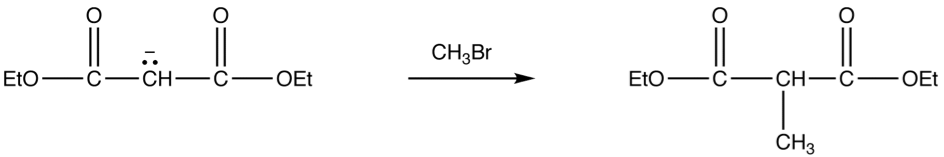
如圖四中的式子,得到烯醇鹽後,再加入鹵烷。會進行取代反應烷基化,建立一個新的碳-碳鍵結。
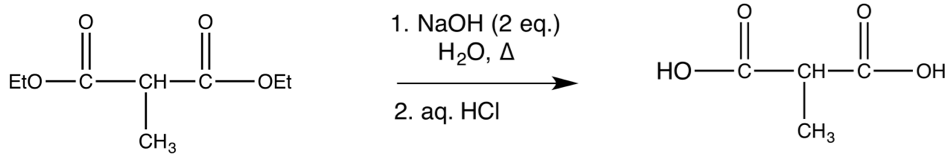
將化合物中的酯基官能基在鹼性水溶液中水解(hydrolysis),可以將酯基酸化得到羧基。(如圖五)
最後,加熱發生脫羧反應(decarboxylation),脫去一分子二氧化碳。(圖六)
另外,若是能在水解之前也可以再重複一次去質子/烷基化的動作,能夠在此化合物的 $$\alpha$$ 位置上,引入另一個相同或不同的烷基。
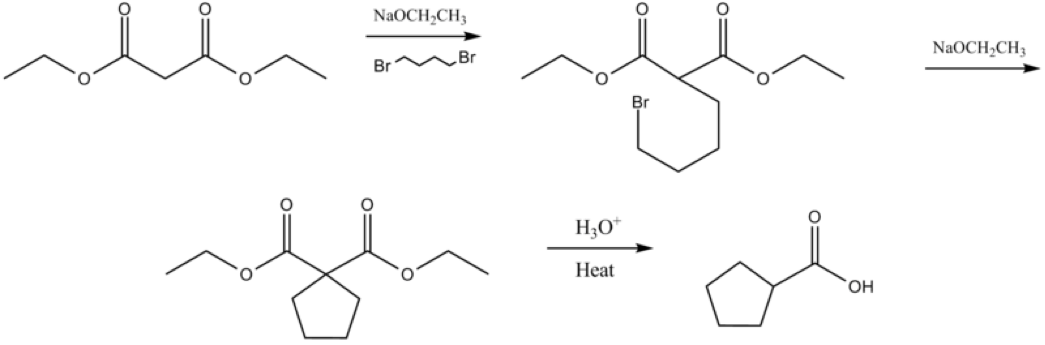
若參與反應的鹵烷為二鹵化物,則可發生分子內丙二酸酯合成反應,並形成環狀酸類。(如圖七)在此情況下,反應亦稱為 Perkin 脂環化合物合成(Perkin alicyclic synthesis)
最後形成的化合物,可視為醋酸在 $$\alpha$$ 位置,建立新的碳-碳鍵結。此方法利用穩定的丙二酸酯進行反應,階段式的引入需要的烷基,可避免多重烷基化,製造含有烷基的羧酸化合物。
參考資料 :
- David R. Klein (2010). Organic Chemistry (1th ed.). New York: John Wiley & Sons, Inc.
- UC Davis Chem Wiki
http://chemwiki.ucdavis.edu/Organic_Chemistry/Reactivity_of_Alpha_Hydrogens/Malonic_Ester_Synthesis - Hubpages
http://online4.hubpages.com/hub/Malonic-Ester-an-Important-Precursor-of-Carboxylic-Acid-Synthesis - Wikipedia
http://en.wikipedia.org/wiki/Malonic_ester_synthesis - UCLA Glossary
http://www.chem.ucla.edu/harding/IGOC/M/malonic_ester_synthesis.html - Pharmaxchange http://pharmaxchange.info/press/2011/02/malonic-ester-synthesis-alkylation-of-enolates/


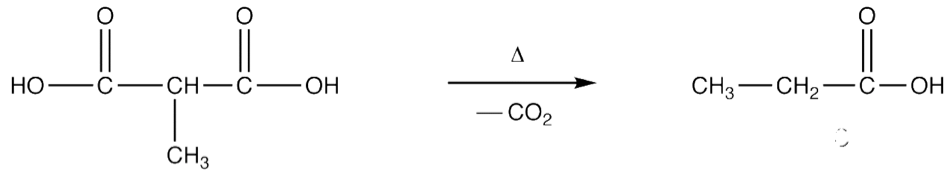
 前一篇文章
前一篇文章 下一篇文章
下一篇文章
