類金屬 ( Metalloids )
類金屬 ( Metalloids )
國立臺灣師範大學化學系碩士班二年級陳筱鳳研究生
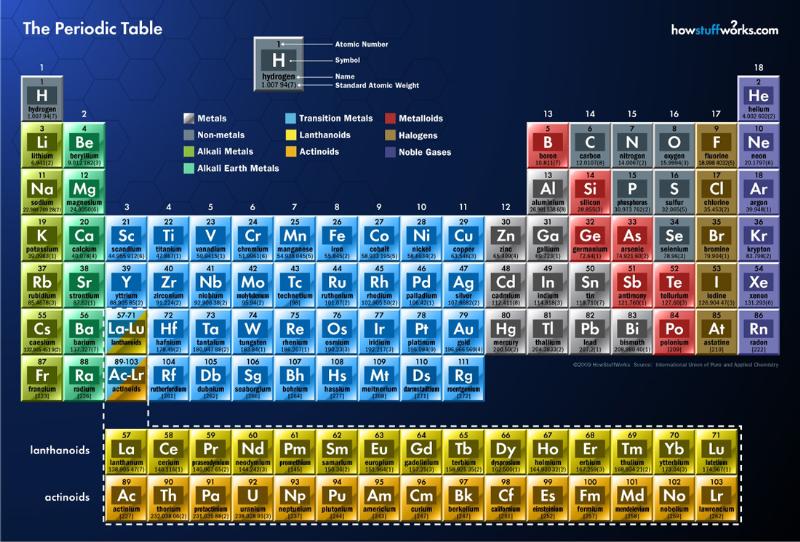
類金屬 ( metalloids ) 是一個用來分類化學元素的名詞。根據它們的物理及化學特性,元素週期表上的化學元素大都可被分類為金屬或非金屬;但有一些元素的性質介於金屬和非金屬之間,僅具有部分金屬或非金屬的性質,即稱為類金屬。[1]
類金屬又稱為準金屬或半金屬。但由於缺少正常金屬的延展性,所以只能算是 ” 半 ” 金屬。分別為硼 ( B ) 、矽 ( Si ) 、鍺 ( Ge ) 、砷 ( As ) 、銻 ( Sb ) 、碲 ( Te ) 這六種元素,而有時釙 ( Po ) 和砈 ( At ) 也被視為類金屬。這類元素的外電子層構型為ns2np 1~5 。在週期表中呈階梯狀的排列,特別的是,這些類金屬元素即使屬於不同族群,也可能會擁有相似的性質。[2]