玻尿酸
玻尿酸 (Hyaluronic acid)
臺北市立第一女子高級中學二年級陳淳、邱雁琳/臺北市立第一女子高級中學化學科周芳妃老師修改/國立臺灣師範大學化學系葉名倉教授責任編輯
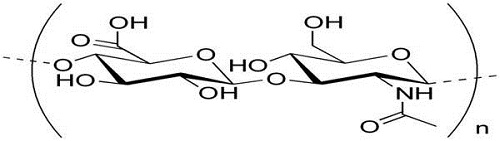
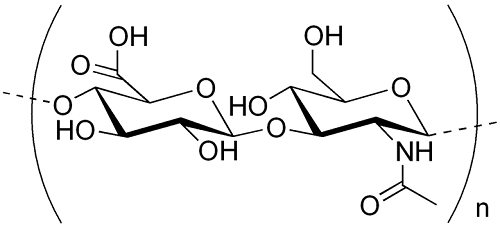
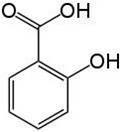
玻尿酸的結構
玻尿酸(Hyaluronic Acid,簡稱HA)又稱玻醣醛酸或透明質酸,是一種天然的酸性多醣體,單體結構為N-乙醯葡糖胺(N-acetyl-D-glucosamine)及D-葡萄糖醛酸(D-glucuronic acid)結合的雙醣體,藉由β-1-3鍵結所鏈結而成的直鏈高分子多醣。透明質酸平均分子量介於100萬到1000萬之間,分子式為(C14H20NNaO11)n,外觀為透明且具黏性的膠狀物質。
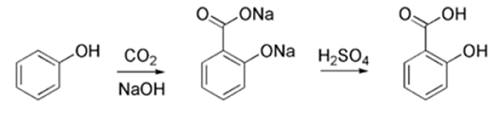
玻尿酸的發現
玻尿酸在1934年美國哥倫比亞大學眼科教授卡爾‧邁耶(Karl‧Meyer)等首先從牛眼玻璃體中分離出。其後發現玻尿酸在自然界中廣泛地存在於脊椎動物之結締組織、黏液組織、眼球之晶狀体及某些細菌的莢膜中。因無論來源為何,其化學組成及結構均相同,使玻尿酸作為醫藥用高分子材料時,具有可被生物体分解吸收的優點。