配位錯合物
配位錯合物 (Coordination Complex)
國立臺灣師範大學附屬中學二年級1322班許羿笙/國立臺灣師範大學附屬高級中學化學科陳昭錦老師
配位錯合物或金屬錯合物是由一個原子或離子(通常是金屬)以及一組環繞在其周圍的鍵結分子或離子構成,後者稱為配位基或錯合劑(complexing agents)。許多含金屬的化合物,尤其是過渡金屬,多半是由配位錯合物組成。
結構
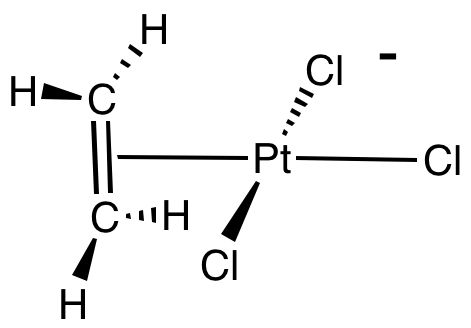
在配位基中與中心原子或離子結合的原子稱為予體原子(donor atom),典型的錯合物均與數個相同或相異的予體原子結合。配位基是以配位共價鍵與中心原子鍵結,配位基將孤對電子提供給中心原子的空軌域,稱為與該原子「配位」。多牙配位基則由數個予體原子組成,其中部分原子與中心原子或離子形成數個配位鍵結,這類錯合物稱為螯合物,其形成的過程稱為螯合(chelation)。配位基可以是無機物,也可以是有機分子,像烯類這類的有機物,能以π鍵與金屬空軌域形成配位鍵,如:Zeise鹽。Zesis鹽的化學式為 K[PtCl3(C2H4)],是最早有記載的有機金屬,也是最先合成出來的烯類錯合物,其錯離子結構如圖一所示。