優養化(Eutrophication)(一)
優養化(Eutrophication)(一)
國立臺灣師範大學附屬高級中學學生蔡韶恬/國立臺灣師範大學附屬高級中學化學科陳昭錦老師
優養化是指水體生態系中,由於清潔劑、肥料或穢物等富含植物生長營養素的物質流入,導致水質汙染的現象,這些植物營養素通常含有氮、磷等元素。
其結果通常使生態系之初級生產力(Primary production)增加(植物過度的生長與腐敗),進一步的影響包括:缺氧、水質惡化及魚、貝類大量死亡等。
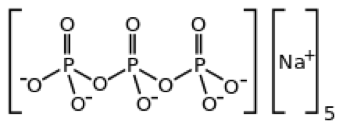
(三聚磷酸鈉曾經是很多種清潔劑的添加成份,為優養化的元兇,圖片來源:http://en.wikipedia.org/wiki/Eutrophication)